生殖医学是为了繁衍还是筛选:IVG(体外配子)进展及风险一览
资讯
2024-01-31
177
全球体外受精市场规模预计将从2023年的244.6亿美元增长到2028年的356.0亿美元,在预测期内(2023-2028年)CAGR为7.80%。 全球人类生殖技术市场预计将以近2%的CAGR增长。不孕症发病率的上升和计划生育的延迟预计将引发市场增长。 在预测期内(2022-2027年),辅助生殖技术市场的CAGR增长率为7.5%。
随着人类生育困难逐步被解决,辅助生殖技术也在快速发展。而除了常见的体外受精、子宫移植等,IVG(体外配子)技术的出现和发展,预示着生殖医学相关研究将进展到一个新的高度。
IVG(体外配子)是什么
IVG是从实验室分化的细胞中复制正常的生殖细胞发育。干细胞保留分化成生物体任何细胞的能力。随着干细胞进一步分化,它们特化并失去其发育潜能。最终,干细胞分化成为生物体的单能细胞。
一种形式的IVG利用在雌性卵母细胞和雄性精子融合后从胚泡的内细胞团收集的胚胎干细胞。这些细胞是多功能的,可以发育成所有胚层的细胞,但不能发育成胚胎外结构(即胎盘)。这些细胞必须在植入前收集。
IVG在动物模型上的研究可能对动物和人类都有益。目前使用动物模型的干细胞和胚胎学研究不受严格法规的约束,使我们能够探索最终应用于人类研究的生物途径。鉴于这项研究在人体上的局限性,动物模型可能是第一个证明IVG应用于癌症幸存者的成功模型。
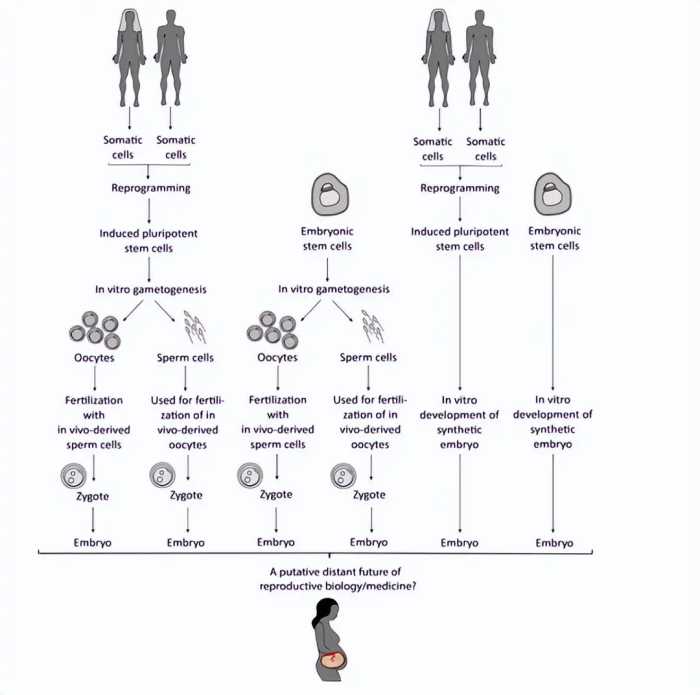
IVG的研究进展与应用前景
2011年有研究使用小鼠模型从多能干细胞成功进行了第一次IVG。从那时起,研究一直在继续发展,现在的重点是从尾尖成纤维细胞衍生的体细胞达成IVG。
目前,这一整个过程已经在体外小鼠模型中完成,也就是说有小鼠在实验室制造的配子中成功诞生。并且已经在恒河猴中成功地从iPSCs分化出PGCLC。
但是这些实验研究进展还不能应用在人类身上。
这种类型的研究在世界范围内仍然是非法的,国际干细胞研究协会(ISSCR)的指导方针还没有将这种研究归入许可类别。因此,这种关于人类使用的讨论已经开始考虑改变和修改目前对胚胎研究的限制。迄今为止,全世界在IVG进行的所有人类胚胎研究都是在14天内的胚胎限制下进行的。
根据目前的规定,IVG来源的生殖细胞需要进行与自然发生的生殖细胞相关的验证研究,以证明其可行性、有效性和安全性。这种验证研究已经开始了。此外,IVG研究还有许多其他活跃的领域,继续有助于我们对人类胚胎的了解。另一项不利用hiPGCLC(卵原细胞和精原细胞)的研究,已经能够研究胚泡样细胞iBlastoids,其来源于体细胞。iBlastoids虽然不能变成胎儿,但确实经历胚胎发生的早期阶段。这将为使用来自人皮肤成纤维细胞的hiPSC进行移植研究。
这些发现表明,IVG的研究可能会更好地理解自然配子发生和胚胎发生的过程,可能会改善不孕症患者的诊断和干预工具。例如,hiPSC成功分化为卵母细胞将提供无数细胞,允许对卵母细胞生物学进行对ART重要的有力研究。这将加速对卵母细胞质量的研究,包括对导致老化(即更易出错的减数分裂和随后的非整倍性)的因素的研究,或评估癌症治疗药物对卵母细胞功能的影响。
IVG的一个独特的应用前景是对患有由特定基因突变引起的疾病的患者的hiPSCs进行基因修饰的潜力,这些患者不希望将这些基因突变遗传给他们的后代。这可能与恶性肿瘤具有特定遗传基础的癌症幸存者患者特别相关。
即使没有像CRISPR这样的基因编辑技术,也有可能创造比目前体外受精实践更大的胚胎池。从这个大得多的库中,可以进行单基因条件的植入前基因检测(PGT-M)。这使得胚胎选择不存在孩子患有上述疾病的风险。同类型的应用前景还包括:避免高龄生育的潜在基因风险和患癌女性的胚胎保存。
最后,也许是IVG潜力中最具突破性的方面,是它改变核心繁殖模式的能力创造新生命需要一个男性和一个女性。也就是说,如果卵原细胞和精原细胞都可以通过来自任一性别的成纤维细胞获得,这可以允许同性夫妇有一个与父母双方都有遗传关系的孩子。
目前,只有一个小鼠模型证明了使用两个雄性配子(精子和卵母细胞)成功活产,这两个配子都来源于雄性小鼠ESCs,尽管精原细胞还没有来源于雌性小鼠,但这项研究仍然在持续探究中。此外,如果卵母细胞和精母细胞由同一人形成,胚胎也可以假设由单个生物亲本形成,如果完成两个或更多个IVG周期,胚胎也可以由两个以上的生物亲本形成。
除了目前IVG面临的生物和监管障碍,IVG及其衍生研究的未来临床应用具有不可估量的潜力。
IVG的应用风险
这种关于IVG潜在后果的不确定性是一种难以预测的风险,现在对其的争论与20世纪70年代末和80年代初第一批同意体外受精妊娠试验的妇女相似,如今对IVG的研究可能会经历类似的最初发生在体外受精中的成功定义的演变。
人们花了40年的时间来理解体外受精成功的定义。体外受精的理想结果已经从早期临床妊娠的最初目标转变为活产,再到生产一个健康的新生儿。未来对体外受精的定义可能是一个来自不太健康的配子或通过IVG来自体细胞的健康婴儿。
此外,通过皮肤收集细胞样本比取卵或收集精子样本的侵入性要小得多,这可能会导致更广泛的人群愿意出售自己的皮肤样本或在未经同意的情况下被采集皮肤样本。既然有复制干细胞而不分化它们的技术,就有可能从一个非常受欢迎的来源产生无限数量的后代,增加了近亲结婚和商业生殖的风险。需要建立法律和法规来规定谁有权使用其他人的干细胞,如果认为这些干细胞在基因上是可取的话。
IVG还挑战了人类生殖最核心的概念之一:胎儿是由一个男性来源的配子和一个女性来源的配子产生的。利用IVG,一个人或一群人可能一起产生一个孩子(例如,通过使用来自两个胚胎的人胚胎干细胞,混合来自四个不同配子的基因,两个胚胎中的每一个都由另外两个体外产生的干细胞制成)。
IVG可能被用来产生大量胚胎,这些胚胎可以进行基因测试,并使用专有算法进行排序,以识别最佳胚胎。这将可能导致一种新的优生学,打造一个更加不平等的世界。出于这个原因,需要有非常明确的规定来阻止可遗传的基因组编辑。目前,卵子供应的短缺对胚胎的遗传选择和操作过程造成了实际的限制。但IVG技术可能会使卵子和胚胎的无限供应成为可能,这可能会大大提高胚胎的遗传选择和基因编辑的速度,以便产生具有理想特征的后代。这种无性生殖方式的广泛使用将最终导致性的终结,至少是为了生殖目的的性会逐渐消亡。
同样的,如果以优生的目的过度使用IVG,不仅可能会加剧对残疾人的现有形式的歧视,而且还会引发新型的基因歧视和等级制度。拥有经济实力的人广泛使用基因选择可能会导致阶级分裂,进一步将社会分成基因有产者和无产者两个阶层。尽管国家支持的优生学对平等构成了严重威胁,但生殖和基因技术领域不受约束的自由市场力量也有可能取得类似的结果。
但是,就目前而言,围绕IVG的研究将继续下去。
1. Stefanie Horerand others, Pluripotent Stem Cell-Derived In Vitro Gametogenesis and Synthetic EmbryosIt Is Never Too Early for an Ethical Debate, Stem Cells Translational Medicine, 2023;, szad042, https://doi.org/10.1093/stcltm/szad042
2. Wesevich, V.G.; Arkfeld, C.; Seifer, D.B. In Vitro Gametogenesis in Oncofertility: A Review of Its Potential Use and Present-Day Challenges in Moving toward Fertility Preservation and Restoration.J. Clin. Med.2023, 12, 3305. https://doi.org/10.3390/jcm12093305
3. Coxir, Sarah Abreu, et al. "From in vivo to in vitro: exploring the key molecular and cellular aspects of human female gametogenesis." Human Cell (2023): 1-29.
声明
本文图文信息来源于网络,旨在进行有价值的医药资讯传播,非商业用途,不作投资推荐和介绍,如有侵权我们将立即处理
本站涵盖的内容、图片、视频等数据系网络收集,部分未能与原作者取得联系。若涉及版权问题,请联系我们删除!联系邮箱:ynstorm@foxmail.com 谢谢支持!
全球体外受精市场规模预计将从2023年的244.6亿美元增长到2028年的356.0亿美元,在预测期内(2023-2028年)CAGR为7.80%。 全球人类生殖技术市场预计将以近2%的CAGR增长。不孕症发病率的上升和计划生育的延迟预计将引发市场增长。 在预测期内(2022-2027年),辅助生殖技术市场的CAGR增长率为7.5%。
随着人类生育困难逐步被解决,辅助生殖技术也在快速发展。而除了常见的体外受精、子宫移植等,IVG(体外配子)技术的出现和发展,预示着生殖医学相关研究将进展到一个新的高度。
IVG(体外配子)是什么
IVG是从实验室分化的细胞中复制正常的生殖细胞发育。干细胞保留分化成生物体任何细胞的能力。随着干细胞进一步分化,它们特化并失去其发育潜能。最终,干细胞分化成为生物体的单能细胞。
一种形式的IVG利用在雌性卵母细胞和雄性精子融合后从胚泡的内细胞团收集的胚胎干细胞。这些细胞是多功能的,可以发育成所有胚层的细胞,但不能发育成胚胎外结构(即胎盘)。这些细胞必须在植入前收集。
IVG在动物模型上的研究可能对动物和人类都有益。目前使用动物模型的干细胞和胚胎学研究不受严格法规的约束,使我们能够探索最终应用于人类研究的生物途径。鉴于这项研究在人体上的局限性,动物模型可能是第一个证明IVG应用于癌症幸存者的成功模型。

IVG的研究进展与应用前景
2011年有研究使用小鼠模型从多能干细胞成功进行了第一次IVG。从那时起,研究一直在继续发展,现在的重点是从尾尖成纤维细胞衍生的体细胞达成IVG。
目前,这一整个过程已经在体外小鼠模型中完成,也就是说有小鼠在实验室制造的配子中成功诞生。并且已经在恒河猴中成功地从iPSCs分化出PGCLC。
但是这些实验研究进展还不能应用在人类身上。
这种类型的研究在世界范围内仍然是非法的,国际干细胞研究协会(ISSCR)的指导方针还没有将这种研究归入许可类别。因此,这种关于人类使用的讨论已经开始考虑改变和修改目前对胚胎研究的限制。迄今为止,全世界在IVG进行的所有人类胚胎研究都是在14天内的胚胎限制下进行的。
根据目前的规定,IVG来源的生殖细胞需要进行与自然发生的生殖细胞相关的验证研究,以证明其可行性、有效性和安全性。这种验证研究已经开始了。此外,IVG研究还有许多其他活跃的领域,继续有助于我们对人类胚胎的了解。另一项不利用hiPGCLC(卵原细胞和精原细胞)的研究,已经能够研究胚泡样细胞iBlastoids,其来源于体细胞。iBlastoids虽然不能变成胎儿,但确实经历胚胎发生的早期阶段。这将为使用来自人皮肤成纤维细胞的hiPSC进行移植研究。
这些发现表明,IVG的研究可能会更好地理解自然配子发生和胚胎发生的过程,可能会改善不孕症患者的诊断和干预工具。例如,hiPSC成功分化为卵母细胞将提供无数细胞,允许对卵母细胞生物学进行对ART重要的有力研究。这将加速对卵母细胞质量的研究,包括对导致老化(即更易出错的减数分裂和随后的非整倍性)的因素的研究,或评估癌症治疗药物对卵母细胞功能的影响。
IVG的一个独特的应用前景是对患有由特定基因突变引起的疾病的患者的hiPSCs进行基因修饰的潜力,这些患者不希望将这些基因突变遗传给他们的后代。这可能与恶性肿瘤具有特定遗传基础的癌症幸存者患者特别相关。
即使没有像CRISPR这样的基因编辑技术,也有可能创造比目前体外受精实践更大的胚胎池。从这个大得多的库中,可以进行单基因条件的植入前基因检测(PGT-M)。这使得胚胎选择不存在孩子患有上述疾病的风险。同类型的应用前景还包括:避免高龄生育的潜在基因风险和患癌女性的胚胎保存。
最后,也许是IVG潜力中最具突破性的方面,是它改变核心繁殖模式的能力创造新生命需要一个男性和一个女性。也就是说,如果卵原细胞和精原细胞都可以通过来自任一性别的成纤维细胞获得,这可以允许同性夫妇有一个与父母双方都有遗传关系的孩子。
目前,只有一个小鼠模型证明了使用两个雄性配子(精子和卵母细胞)成功活产,这两个配子都来源于雄性小鼠ESCs,尽管精原细胞还没有来源于雌性小鼠,但这项研究仍然在持续探究中。此外,如果卵母细胞和精母细胞由同一人形成,胚胎也可以假设由单个生物亲本形成,如果完成两个或更多个IVG周期,胚胎也可以由两个以上的生物亲本形成。
除了目前IVG面临的生物和监管障碍,IVG及其衍生研究的未来临床应用具有不可估量的潜力。
IVG的应用风险
这种关于IVG潜在后果的不确定性是一种难以预测的风险,现在对其的争论与20世纪70年代末和80年代初第一批同意体外受精妊娠试验的妇女相似,如今对IVG的研究可能会经历类似的最初发生在体外受精中的成功定义的演变。
人们花了40年的时间来理解体外受精成功的定义。体外受精的理想结果已经从早期临床妊娠的最初目标转变为活产,再到生产一个健康的新生儿。未来对体外受精的定义可能是一个来自不太健康的配子或通过IVG来自体细胞的健康婴儿。
此外,通过皮肤收集细胞样本比取卵或收集精子样本的侵入性要小得多,这可能会导致更广泛的人群愿意出售自己的皮肤样本或在未经同意的情况下被采集皮肤样本。既然有复制干细胞而不分化它们的技术,就有可能从一个非常受欢迎的来源产生无限数量的后代,增加了近亲结婚和商业生殖的风险。需要建立法律和法规来规定谁有权使用其他人的干细胞,如果认为这些干细胞在基因上是可取的话。
IVG还挑战了人类生殖最核心的概念之一:胎儿是由一个男性来源的配子和一个女性来源的配子产生的。利用IVG,一个人或一群人可能一起产生一个孩子(例如,通过使用来自两个胚胎的人胚胎干细胞,混合来自四个不同配子的基因,两个胚胎中的每一个都由另外两个体外产生的干细胞制成)。
IVG可能被用来产生大量胚胎,这些胚胎可以进行基因测试,并使用专有算法进行排序,以识别最佳胚胎。这将可能导致一种新的优生学,打造一个更加不平等的世界。出于这个原因,需要有非常明确的规定来阻止可遗传的基因组编辑。目前,卵子供应的短缺对胚胎的遗传选择和操作过程造成了实际的限制。但IVG技术可能会使卵子和胚胎的无限供应成为可能,这可能会大大提高胚胎的遗传选择和基因编辑的速度,以便产生具有理想特征的后代。这种无性生殖方式的广泛使用将最终导致性的终结,至少是为了生殖目的的性会逐渐消亡。
同样的,如果以优生的目的过度使用IVG,不仅可能会加剧对残疾人的现有形式的歧视,而且还会引发新型的基因歧视和等级制度。拥有经济实力的人广泛使用基因选择可能会导致阶级分裂,进一步将社会分成基因有产者和无产者两个阶层。尽管国家支持的优生学对平等构成了严重威胁,但生殖和基因技术领域不受约束的自由市场力量也有可能取得类似的结果。
但是,就目前而言,围绕IVG的研究将继续下去。
1. Stefanie Horerand others, Pluripotent Stem Cell-Derived In Vitro Gametogenesis and Synthetic EmbryosIt Is Never Too Early for an Ethical Debate, Stem Cells Translational Medicine, 2023;, szad042, https://doi.org/10.1093/stcltm/szad042
2. Wesevich, V.G.; Arkfeld, C.; Seifer, D.B. In Vitro Gametogenesis in Oncofertility: A Review of Its Potential Use and Present-Day Challenges in Moving toward Fertility Preservation and Restoration.J. Clin. Med.2023, 12, 3305. https://doi.org/10.3390/jcm12093305
3. Coxir, Sarah Abreu, et al. "From in vivo to in vitro: exploring the key molecular and cellular aspects of human female gametogenesis." Human Cell (2023): 1-29.
声明
本文图文信息来源于网络,旨在进行有价值的医药资讯传播,非商业用途,不作投资推荐和介绍,如有侵权我们将立即处理
本站涵盖的内容、图片、视频等数据系网络收集,部分未能与原作者取得联系。若涉及版权问题,请联系我们删除!联系邮箱:ynstorm@foxmail.com 谢谢支持!










